Estry to związki organiczne powstające w wyniku reakcji alkoholu z kwasem (reakcji estryfikacji).
Wzór ogólny estrów: R1COOR2
½½
Grupa funkcyjna estrów: - C – O
Reakcja estryfikacji.
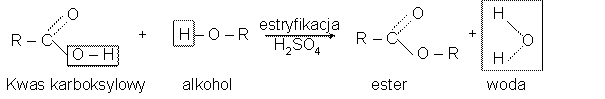
Mechanizm reakcji estryfikacji został ustalony dzięki wykorzystaniu metody izotopowej. Przeprowadzono estryfikację kwasu benzoesowego metanolem znaczonym izotopem tlenu 18O. Badając produkty reakcji, stwierdzono, że izotop ten znajdował się w otrzymanym estrze. Nie wykryto natomiast jego obecności w cząsteczkach wody. Cząsteczka wody w reakcji estryfikacji powstaje więc z grupy hydroksylowej cząsteczki kwasu i wodoru cząsteczki alkoholu.
Nazwy estrów składają się z dwóch wyrazów. Pierwszy z nich pochodzi od nazwy kwasu, z którego powstał dany ester. Ester kwasu mrówkowego to mrówczan, octowego – octan, propionowego – propionian, masłowego – maślan itd. Drugi wyraz wywodzi się od określenia alkilu pochodzącego z alkoholu tworzącego ester, np. alkohol metylowy daje człon metylu, alkohol etylowy – etylu, alkohol propylowy – propylu itd.

mrówczan metylu
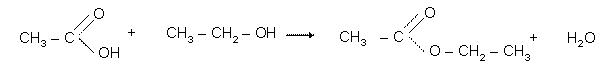
octan etylu

octan metylu
Pod wpływem katalizatorów zasadowych w postaci odpowiednich alkoholanów estry reagują z alkoholami. Reakcja ta jest odwracalna, nosi nazwę alkoholizy lub transestryfikacji. Wykorzystuje się ją do otrzymywania estrów i alkoholi. Alkoholiza octanu etylu propanolem:
O O
½½ C3H7OH- Na+ ½½
CH3 – C – O – CH2 – CH3 + C3H7OH ----------→ CH3 – C – O – C3H7 + CH3CH2OH
octan etylu propanol octan propylu etanol
Reakcja estryfikacji jest reakcją odwracalną. Proces odwrotny do niej to hydroliza, zachodząca pod wpływem wody.
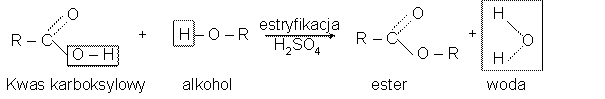
Hydroliza prowadzi do powstania kwasu i alkoholu. Hydroliza estrów zachodzi zarówno pod wpływem kwasów, jak i zasad. Hydroliza w środowisku kwasowym jest reakcją odwracalną. Kationy wodoru katalizują tę reakcję, nie zużywając się w niej. Hydroliza octanu etylu w środowisku kwasowym:
O O
½½ H+ ½½
CH3 – C – O – CH2 – CH3 + H2O ----------→ CH3 – C –OH + CH3CH2OH
octan etylu kwas octowy etanol
W środowisku zasadowym hydroliza jest reakcją nieodwracalną. Przebiega do wyczerpania substratów. Hydroliza octanu etylu w środowisku zasadowym:
O O
½½ ½½
CH3 – C – O – CH2 – CH3 + NaOH ----------→ CH3 – C –ONa + CH3CH2OH
octan etylu etanolan sodu etanol
Małocząsteczkowe estry są związkami o bardzo przyjemnych zapachach. Zapach estrów zanika wraz ze wzrostem długości łańcucha węglowego kwasów i alkoholi użytych do ich produkcji (od przyjemnie pachnących cieczy do prawie bezwonnych wosków, np. wosk pszczeli, oraz tłuszczów, np. smalec, łój).
Zapachy estrów:
- maślan butylu – zapach ananasów
- maślan metylu – zapach jabłek
- mrówczan benzylu – zapach jaśminu
- mrówczan etylu – zapach rumu
- mrówczan izobutylu – zapach malin
- octan amylu – zapach bananów
- octan izoamylu – zapach gruszek
- octan oktylu – zapach pomarańcz
- octan izobutylu – zapach gruszek, agrestu
- salicylan metylu – zapach baldaszkowatych
Szczególną grupę estrów stanowią tłuszcze. Tłuszcze to grupa związków zróżnicowanych zarówno pod względem budowy, jak i właściwości.
Podział tłuszczów prostych ze względu na pochodzenie:
Tłuszcze proste:
- roślinne
- zwierzęce
Podział tłuszczów prostych ze względu na stan skupienia:
Tłuszcze proste:
- ciekłe
- stałe
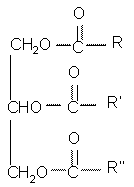
Tłuszcze proste są estrami glicerolu i kwasów karboksylowych o długich (najczęściej) łańcuchach węglowych, tzw. kwasów tłuszczowych. Naturalne tłuszcze zawierają przeważnie reszty węglowodorowe pochodzące z różnych kwasów karboksylowych.
Wzór ogólny tłuszczów:
Tłuszcze, będące związkami niepolarnymi, nie rozpuszczają się w wodzie, rozpuszczają się natomiast w rozpuszczalnikach niepolarnych, np. w benzynie. Gęstość tłuszczów jest mniejsza niż gęstość wody, dlatego pływają one po jej powierzchni. Stanowią mieszaniny, nie mają więc ściśle określonej temperatury topnienia. Topnieją w pewnym przedziale temperaturowym. W cząsteczkach ciekłych tłuszczów roślinnych między atomami węgla występują wiązania podwójne – dlatego cząsteczki te ulegają reakcjom przyłączania
(addycji). Odbarwiają np. wodę bromową, przyłączając zawarty w niej brom. W przemyśle spożywczym ciekłe tłuszcze roślinne przekształca się w tłuszcze stałe. Proces ten polega na przyłączaniu wodoru do wiązań wielokrotnych obecnych w cząsteczkach estrów tworzących tłuszcz. Przeprowadza się go w obecności katalizatora niklowego i nazywa utwardzaniem (uwodornieniem) tłuszczów. Uwodornione tłuszcze służą do produkcji margaryn – emulsji otrzymywanych z utwardzanych olejów roślinnych, wzbogacanych witaminami A i E oraz substancjami poprawiającymi smak, zapach i trwałość gotowego produktu. Trwałość margaryny zapewnia lecytyna, odgrywająca rolę emulgatora.
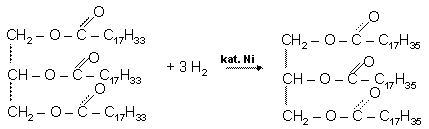
Zmydlanie tłuszczów
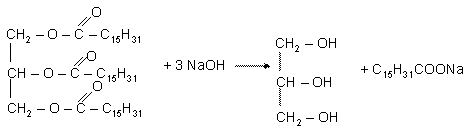
Gorsze gatunki tłuszczów są stosowane do produkcji mydła. Proces ten nosi nazwę zmydlania tłuszczów.
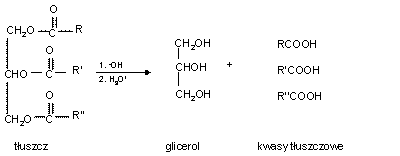
Hydroliza tłuszczów w organizmach żywych. Podczas procesów trawiennych tłuszcze ulegają hydrolizie pod wpływem enzymów zwanych lipazami, występujący w wydzielinie trzustki i wątroby. Powstające kwasy tłuszczowe ulegają dalszemu rozkładowi i utlenianiu, tworząc ostatecznie tlenek węgla(IV), wodę oraz dużą ilość energii potrzebnej do prawidłowego funkcjonowania organizmu.
Tłuszcz + woda --lipaza--→ kwasy tłuszczowe + glicerol
Spożywanie nadmiernych ilości tłuszczów prowadzi do otyłości, ponieważ odkładają się one w postaci tkanki tłuszczowej. Szczególną grupę estrów stanowią tłuszcze. Tłuszcze to grupa związków zróżnicowanych zarówno pod względem budowy, jak i właściwości.
WOSKI – dawniej określane jako estry wyższych kwasów tłuszczowych z wyższymi alkoholami jednowodorotlenowymi, obecnie pojęcie wosków rozszerzyło się, obejmując szereg substancji o podobnych właściwościach fizycznych. Są to przeważnie mieszaniny, które mogą zawierać węglowodory parafinowe i ich pochodne: alkohole, ketony, kwasy, etery i estry, niekiedy również związki aromatyczne. Topią się w temp. powyżej 40° bez rozkładu tworząc ciecz o małej lepkości. Woski dzieli się ma naturalne i syntetyczne. Stosowane są do wyrobu past do podłóg i do butów, w przemyśle kosmetycznym (pomadki, kremy itp.) i do wyrobu artykułów biurowych (kredki). Ponadto są wykorzystywane w przemysłach elektrotechnicznym, gumowym, farb i lakierów, opakowań, do wyrobu świec woskowych, wosków dentystycznych, wosków do modelowania, artykułów pomocniczych w przemyśle tekstylnym.
Woski syntetyczne otrzymuje się metodą chemicznej przemiany wosków naturalnych oraz właściwe woski syntetyczne, np. estry wytworzone z kwasów alkoholi otrzymanych z węglowodorów.


