Atom- najmniejsza część pierwiastka chemicznego, reprezentująca jego właściwości. Jest cząstką elektrycznie obojętną. Składa się jądra atomowego, wewnątrz którego znajdują się dodatnio naładowane protony i pozbawione ładunku neutrony oraz przebywające w przestrzeni wokół jądra ujemnie naładowane elektrony.
Cząstki elementarne:
- protony - cząstki o dodatnim ładunku elektrycznym i masie 1 [u] = 1,67∙10-27[kg];
- neutrony - cząstki pozbawione ładunku elektrycznego o masie 1 [u] = 1,67∙10-27[kg];
- elektrony - cząstki o ujemnym ładunku elektrycznym i masie 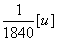 , uznaje się jego masę za równą 0.
, uznaje się jego masę za równą 0.
Każdy atom jest scharakteryzowany za pomocą dwóch liczb: liczby masowej i liczby atomowej:
- Liczba atomowa (Z) - określa liczbę protonów w jądrze atomowym danego pierwiastka.
- Liczba masowa (A) - określa sumaryczną liczbę protonów i neutronów w danym jądrze atomowym.
Izotop - odmiana danego pierwiastka o identycznej liczbie atomowej, ale rożnej liczbie neutronów znajdujących się w jądrze atomowym.
Izotopy występują w przyrodzie naturalnie lub też są sztucznie otrzymywane. Niektóre z nich są trwałe, inne są nie trwałe i łatwo ulegają rozpadowi promieniotwórczemu.
Zastosowanie izotopów:
- określenie wieku wykopalisk organicznych za pomocą izotopu węgla 14C.
- w medycynie - radioterapie (60Co)
- w chemii - badanie mechanizmów reakcji, określanie rozpuszczalności substancji trudno rozpuszczalnych.
-paliwo w reaktorach jądrowych (235U, 239U)
Mol - miara ilości substancji, która zawiera tyle elementów, ile znajduje się w 12 g izotopu węgla 12C.
Masa molowa - masa jednego mola substancji wyrażona w gramach.
Liczba Avogadra - liczba elementów zawarta w 1 molu substancji, liczbowo wynosi: 6,02∙1023.
Substancja chemiczna - każda materia, którą może opisać chemia, podając jej właściwości fizyczne i chemiczne. Wśród nich wyróżniamy:
- Pierwiastek chemiczny - to zbiór atomów o jednakowych właściwościach fizycznych i chemicznych. Jest uznawany za substancję prostą, czyli substancję, której nie da się rozłożyć na prostsze czynniki.
- Związek chemiczny - to zbiór cząsteczek o jednakowych właściwościach fizycznych i chemicznych. Jest uznawany za substancję złożoną, czyli substancję, którą da się rozłożyć na prostsze czynniki (pierwiastki).
- Mieszaniny - substancje chemiczne powstałe przez mechaniczne zmieszanie przynajmniej dwóch substancji (nie dochodzi między nimi do reakcji chemicznej). Można je podzielić na:
- mieszaniny jednorodne (homogeniczne) - składników mieszaniny nie da się rozróżnić po zmieszaniu, nawet pod mikroskopem
Np. sól + woda; mleko + cukier; alkohol + ocet
- mieszaniny niejednorodne (heterogeniczne) - składniki mieszaniny można rozróżnić po zmieszaniu.
Np. opiłki żelaza + mak; piasek + siarka
Chemia jest nauką zajmującą się budową i właściwościami związków chemicznych. Z tego względu chemię można podzielić na dwie gałęzie:
- Chemię nieorganiczną - zajmuje się właściwościami i przemianami wszystkich pierwiastków chemicznych oraz ich związków, z wyjątkiem związków węgla.
Najważniejsze grupy związków nieorganicznych:
- tlenki
- wodorki
- kwasy
- wodorotlenki metali
- sole
- Chemia organiczna - zajmuje się właściwościami i przemianami związków węgla.
Najważniejsze grupy związków organicznych:
- węglowodory (nasycone, nienasycone, aromatyczne)
- fluorowco pochodne węglowodorów
- alkohole
- aldehydy i ketony
- kwasy karboksylowe
- estry
- etery
- nitrozwiązki
- aminy i amidy
- aminokwasy i białka
- cukry (monosacharydy, disacharydy i polisacharydy)
- tłuszcze (nasycone i nienasycone)


