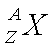
LICZBA ATOMOWA (Z) - określa liczbę protonów w jądrze atomowym;
jednocześnie jest numerem pierwiastka w układzie pierwiastkowym
LICZBA MASOWA (A) – określa sumę nukleonów (protonów i neutronów) w jądrze atomowym
ATOM - najmniejsza część pierwiastka chemicznego zachowująca jego właściwości;
tworzy układ elektrycznie obojętny, składający się dodatnio naładowanego jądra atomowego oraz krążących wokół niego ujemnie naładowanych elektronów
PROTON – cząstka elementarna, wchodząca w skład jądra atomowego, obdarzona dodatnim ładunkiem; jego masa równa jest 1 [u]
NEUTRON - cząstka elementarna, wchodząca w skład jądra atomowego, elektrycznie obojętna; jego masa równa jest 1 [u]
ELEKTRON - cząstka elementarna, znajdująca się w przestrzeni wokół jądra atomowego, obdarzona ujemnym ładunkiem; jego masa równa jest 1/1830 [u]
ELEKTRONY WALENCYJNE – elektrony znajdujące się na ostatniej powłoce elektronowej; ich liczbę w atomie określa numer grupy danego pierwiastka
JON – atom lub cząsteczka obdarzona ładunkiem elektrycznym
ANION - jon o ładunku ujemnym
KATION - jon o ładunku dodatnim
ATOMOWA JEDNOSTKA MASY (u)- masa równa 1/12 masy 1 atomu węgla (1 u = 1,67 ∙ 10-24 g )
IZOTOPY - odmiany danego pierwiastka o jednakowej liczbie atomowej, różniące się liczbą neutronów w jądrze
WIĄZANIE KOWALENCYJNE (atomowe)- wiązanie polegające na łączeniu się atomów przez uwspólnienie par elektronowych.
WIĄZANIE JONOWE - wiązanie polegające na przekazaniu elektronów pochodzących od jednego atomu, drugiemu atomowi
WARTOŚCIOWOŚĆ – liczba wiązań chemicznych wytworzonych przez dany atom
WZÓR SUMARYCZNY – za pomocą niego określamy liczbę i rodzaj atomów wchodzących w skład cząsteczki
WZÓR KRESKOWY – za pomocą niego określamy liczbę, rodzaj atomów oraz strukturę wiązań wchodzących w skład cząsteczki.
RÓWNANIE REAKCJI CHEMICZNEJ – opis reakcji za pomocą wzorów chemicznych
PRAWO ZACHOWANIA MASY – sumaryczna masa substratów reakcji chemicznej musi być równa sumarycznej masie produktów powstałych, w czasie tej reakcji.
PRAWO STAŁOŚCI SKŁADU – stosunek mas pierwiastków wchodzących w skład związku chemicznego jest wielkością stałą.
PRAWO OKRESOWOŚCI – właściwości chemiczne i fizyczne pierwiastków uporządkowanych według wzrastającej liczby atomowej , powtarzają się okresowo.


