Reakcja chemiczna – przemiana, w trakcie której z jednych składników układu (substratów) powstają inne składniki (produkty), o odmiennych właściwościach fizycznych i chemicznych.
Reagent (substancja reagująca) – jest to substancja podlegająca reakcjom chemicznym. Reagentem można nazwać substrat, ale także produkt.
- Podstawowy podział reakcji chemicznych:
- Reakcje syntezy, czyli łączenia się, zachodzą wtedy, gdy z kilku substratów powstaje jeden produkt
Schematycznie można to zapisać: X + Y → XY
Np. SO2 + H2O → H2SO4
- Reakcje analizy, czyli rozkładu, zachodzą wtedy, gdy z jednego substratu powstaje kilka produktów.
Schematycznie można to zapisać: XY → X + Y
Np. CaCO3 → CO2 + CaO
- Reakcje wymiany, zachodzą wtedy, gdy substraty wymieniają się pierwiastkami, lub grupami pierwiastków. Wśród nich wyróżniamy:
- Reakcje wymiany pojedynczej, czyli wypieranie przez bardziej aktywny pierwiastek pierwiastka mniej aktywnego ze związku chemicznego.
Schematycznie można to zapisać: X + AB → XB + A
Np. 2 Na + MgCl2 → 2 NaCl + Mg
- Reakcje wymiany podwójnej, czyli reakcja dwóch związków chemicznych, w wyniku której produktami zostają dwa nowe związki chemiczne Schematycznie można to zapisać: XY + AB → XB + AY
Np. 2 NaOH +H2SO4→ Na2SO4 + 2 H2O
Reakcja odwracalna – to reakcje mające możliwość przebiegania w obie strony tzn. zarówno ze substratów w produkty, jak i z produktów w substraty. Przy zapisie takiej reakcji używa się symbolu dwóch strzałek : jednej skierowanej w prawo, drugiej w lewo.
Uważa się, że wszystkie reakcje chemiczne są odwracalne, a ich przebieg zależy od warunków przeprowadzania reakcji. W mieszaninie poreakcyjnej zawsze znajdują substraty oraz produkty, o różnych stężeniach. Ich proporcje określa stała równowagi reakcji (K). Reakcje, które potocznie określa się za nieodwracalne, to takie, które w określonych warunkach zachodzą z prawie 100% wydajnością (np. strącanie trudno rozpuszczalnych osadów).
Uwaga! Należy unikać określenia „reakcja nieodwracalna”, zastępując je wyrażeniem „reakcja praktycznie nieodwracalna”.
Reakcje równoległe – Z reakcjami równoległymi można się spotkać, gdy z jednych substratów, w wyniku reakcji chemicznej mogą powstawać równocześnie różne produkty. Reakcje te są w stosunku do siebie konkurencyjne. Czasem ilościowo jest więcej jednych produktów od drugich, wtedy mówi się o produktach głównych (i reakcji głównej) oraz o produktach ubocznych ( i reakcji ubocznej).
- Typy reakcji chemicznych:
- Reakcja substytucji (inaczej: reakcja podstawienia)
Reakcja, w czasie której następuje wymiana atomu lub grupy atomów w jednej cząsteczce na inny atom lub grupę atomów pochodzących z innej cząsteczki. Ten typ reakcji jest często spotykany w chemii organicznej. Przykładem może być substytucja węglowodorów nasyconych fluorowcami:
CH3 – CH2 – CH3 + Br2 → CH3 – CH2 – CH2Br + HBr
W chemii organicznej są rozróżniane, ze względu na charakter odczynnika atakującego różne typy reakcji podstawienia:
- Substytucja rodnikowa, gdy odczynnikiem atakującym jest rodnik
Rodnik to atom lub grupa atomów posiadająca niesparowany elektron, np. H∙, ∙OH, ∙Cl, ∙CH3
Przykład takiej reakcji to podana już substytucja węglowodorów nasyconych fluorowcami, zachodząca pod wpływem światła, które powoduje rozkład fluorowców na rodniki
Cl2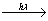 Cl∙ + ∙Cl
Cl∙ + ∙Cl
CH3 – CH2 – CH3 + ∙Cl → CH3 – CH2 – CH2∙ + HCl
CH3 – CH2 – CH2∙ + ∙Cl → CH3 – CH2 – CH2Cl
- Substytucja nukleofilowa, gdy odczynnikiem atakującym jest nukleofil.
Nukleofil to ujemny jon lub cząsteczka posiadająca wolna parę elektronową.
- Substytucja elektrofilowa, gdy odczynnikiem atakującym jest elektrofil
Elektrofil to dodatni jon lub cząsteczka posiadająca lukę elektronową.
Przykładem substytucji elektrofilowej jest podstawienie atomów wodoru w pierścieniu aromatycznym innymi podstawnikami. Jeżeli w pierścieniu benzenowym obecne są już jakieś podstawniki, to mają one wpływ na podstawienie kolejnych. Z tego względu wyróżniamy:
- podstawniki I rodzaju – następny podstawnik kierują w pozycję orto (1,2-) oraz para (1,4-)
Np. grupy alkilowe, grupy aminowe, fluorowce, grupy hydroksylowe
- podstawniki II rodzaju – następny podstawnik kierują w pozycję meta (1,3-)
Np. grupy karboksylowe, grupy nitrowe, grupy sulfonowe
- Reakcja addycji (inaczej: reakcja przyłączenia)
Reakcja, w czasie której następuje przyłączenie się jednej cząsteczki do drugiej kosztem zerwania wiązania wielokrotnego (zazwyczaj obniża się krotność tego wiązania)
Przykładem może być reakcja addycji fluorowców do alkenów.
CH2=CH–CH3 + Cl2 → CH2Cl-CHCl-CH3
Oraz inne:
CH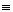 CH + HCl → CHCl=CH2
CH + HCl → CHCl=CH2
- Reakcja eliminacji
Reakcja, w czasie której następuje, podwyższenie krotności wiązania. Stanowi reakcje odwrotną w stosunku do reakcji przyłączania.
Przykładem może być reakcja eliminacji alkoholu
CH3-CH2OH → CH2=CH2 + H2O
Reakcja barwna - reakcja, w czasie której następuje zmiana barwy składników; produkt(y) mają inny kolor od substratów. Zachodzenie takiej zmiany jest często wykorzystywane w analizie chemicznej do identyfikacji oraz oznaczania ilości substancji.
Reakcja łańcuchowa – reakcja przebiegająca przez szereg następujących po sobie etapów, nazywanych łańcuchem reakcji. Produkt każdego z etapów reakcji łańcuchowej jest jednocześnie substratem kolejnego etapu. Przykładem reakcji łańcuchowej jest reakcja substytucji rodnikowej, w której rodnik jest jej inicjatorem. Substytucja alkanów zachodzi pod wpływem światła, które powoduje powstawanie rodników fluorowców.
Np. C2H6 + Cl2 → C2H5Cl + HCl
C2H5Cl + Cl2 → C2H4Cl2 + HCl
C2H4Cl2 + Cl2 → C2H3Cl3 + HCl
C2H3Cl3 + Cl2 → C2H2Cl4 + HCl
C2H2Cl4 + Cl2 → C2HCl5 + HCl
C2HCl5 + Cl2 → C2Cl6 + HCl
Reakcja jądrowa także może być przykładem reakcji łańcuchowej. Dzieje się tak m.in. w bombie atomowej. Jeżeli zbombarduje się ciężkie jądra atomowe neutronami, to zajdzie reakcja jądrowa, w wyniku której powstanie nowe jądro atomowe oraz wolne neutrony, które spowoduję rozszczepienie następnych jąder. Przy każdej z tych reakcji wyzwalana jest energia; znajduje ona zastosowanie przy budowie reaktorów jądrowych lub broni atomowej.
- Wybrane przykłady reakcji chemicznych
- Synteza Wurtza- reakcja fluorowcopochodnych alkilowych z sodem, w wyniku której powstają węglowodory nasycone. Reakcja ta jest wykorzystywana do otrzymywania symetrycznych alkanów.
- Reakcja Fittiga - reakcja fluorowcopochodnych arylowych z sodem, w wyniku której powstają węglowodory aromatyczne.
- Reakcja Cannizzaro – charakterystyczna reakcja, zachodząca dla aldehydów, przeprowadza się ją w środowisku zasadowym. Produktami tej reakcji są alkohol oraz anion kwasu karboksylowego.


