Wolne atomy mogą, za pomocą oddziaływań zwanych wiązaniami chemicznymi, zostać powiązane w większe zgrupowania - cząsteczki.
Istnieje kilka typów oddziaływań, różniących się między sobą siłą wiązania. Twa główne typy to wiązania silne - kowalencyjne oraz wiązania słabe. Pierwsze z nich są bardzo trwałe w temperaturach fizjologicznych, drugie natomiast, w przypadku gdy występują pojedynczo, ulegają łatwemu zerwaniu nawet w niskich temperaturach. Duże znaczenie mają natomiast wiązania słabe występujące grupowo. Siła wiązania zależy od odległości związanych atomów - im atomy są dalej, tym wiązanie jest słabsze.
Układy biologiczne charakteryzują się dużą różnorodnością występujących w nich wiązań chemicznych. Istotną rolę odgrywają tu zarówno silne i stabilne wiązania kowalencyjne jak i słabe wiązania niekowalencyjne, które stabilizują wiele struktur biologicznych, takich jak białka, kwasy nukleinowe i błony komórkowe.
Wiązanie kowalencyjne opiera się na zjawisku uwspólniania par elektronów między dwoma silnie elektroujemnymi atomami, z których każdy dąży do przyłączenia obu elektronów. Wyróżniamy dwa typy wiązań kowalencyjnych:
- spolaryzowane - wiązaniem jest wspólna para elektronów przesunięta w kierunku bardziej elektroujemnego atomu, w wyniku czego na jednym z atomów wytwarza się cząstkowy ładunek dodatni, a na drugim ujemny. Wiązanie kowalencyjne spolaryzowane powstaje między atomami pierwiastków niemetalicznych, różniących się elektroujemnością o 0 - 1,7 w skali Paulinga. Cząsteczki z takim wiązaniem mogą być zarówno dipolami (np. HCl, H2O) jak i obojętne (np. CO2)
- niespolaryzowane - tworzone przez dwa identyczne fragmenty, np. O - O, Cl - Cl, H3C - CH3. Obydwa wiązane atomy są jednakowo elektroujemne i każdy z nich tak samo silnie przyciąga pary elektronów.
Substancje kowalencyjne w stanie stałym mogą tworzyć dwa rodzaje kryształów:
- cząsteczkowe (molekularne) - zbudowane z wielu cząsteczek, podczas topnienia lub rozpuszczania rozpadają się na osobne cząsteczki.
- kowalencyjne - zbudowane z atomów połączonych wiązaniami kowalencyjnymi w jedną wielką "cząsteczkę". Ten typ kryształu występuje znacznie częściej, np. diament, krzem, węglik krzemu.
Właściwości substancji kowalencyjnych
Zarówno w stanie ciekłym, jak i stałym, substancje zbudowane z atomów połączonych wiązaniami kowalencyjnymi są izolatorami elektrycznymi - nie przewodzą prądu. Powodem tego jest brak dysocjacji elektrolitycznej oraz swobodnych elektronów mogących uczestniczyć w procesie przewodzenia prądu. Jedynym wyjątkiem jest grafit. Domieszkowane (zanieczyszczone) substancje kowalencyjne mogą być bardzo dobrymi półprzewodnikami.
Cząsteczki kowalencyjne spolaryzowane rozpuszczają się jedynie w polarnych rozpuszczalnikach, na przykład wodzie, natomiast niespolaryzowane - w rozpuszczalnikach niepolarnych.
Substancje zawierające wiązania kowalencyjne reagują z innymi związkami wolno, gdyż konieczne jest dostarczenie dużej energii do zerwania wiązania. Z tego samego powodu związki tworzące kryształy molekularne mają znacznie niższe temperatury topnienia i wrzenia niż kryształy kowalencyjne.
Wiązania wodorowe
Atom wodoru, ze względu na to, iż ma tylko jeden elektron, może tworzyć tylko jedno wiązanie kowalencyjne. Jest on jednak zdolny do tworzenia innego typu wiązania, znacznie słabszego - wiązania wodorowego, polegającego na słabym oddziaływaniu elektrostatycznym pomiędzy silnie elektroujemnym atomem (akceptorem wiązania wodorowego) a atomem wodoru związanym kowalencyjnie z innym silnie elektroujemnym atomem (donorem wiązania wodorowego). We wzorach chemicznych wiązanie wodorowe oznacza się linią przerywaną: N - H . . . . O.
Wiązania wodorowe odgrywają zasadniczą rolę w wielu układach biologicznych. Jednym z najważniejszych z nich jest woda - spolaryzowane cząsteczki H2O silnie oddziałują ze sobą za pomocą wiązań wodorowych. Dzięki istnieniu wiązań wodorowych lekkie cząsteczki wody nie ulatniają się już w niskich temperaturach, tylko tworzą stan ciekły - dopiero w 100°C woda zaczyna przechodzić w stan gazowy. Również lód zbudowany jest z cząsteczek H2O połączonych siecią wiązań wodorowych:
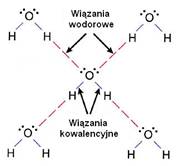
http://witcombe.sbc.edu/water/
Inne ważne funkcje wiązań wodorowych to zwiększanie rozpuszczalności związków i tworzenie trójwymiarowych struktur makrocząsteczek - białek, kwasów nukleinowych, DNA.
Wiązania jonowe to kolejny typ wiązań chemicznych zaliczanych do słabych. Wiązanie takie tworzy się w wyniku przyciągania elektrostatycznego pomiędzy anionem - atomem (fragmentem cząsteczki) posiadającym ładunek ujemny, oraz kationem - atomem zawierającym ładunek dodatni, gdy różnica elektroujemności jest większa niż 1,7 w skali Paulinga. Jony mogą powstawać w wyniku zerwania wiązania kowalencyjnego - bardziej elektroujemny fragment "zabiera" obydwa elektrony (anion), natomiast mniej elektroujemny fragment staje się kationem. Przykładem cząsteczki jonowej jest NaCl, w której różnica elektroujemności jest tak duża (Na 0,9, Cl 3,0), że chmura elektronów zostaje całkowicie przeciągnięta na stronę chloru - rozkład ładunku wygląda następująco: Na+Cl- .
Właściwości substancji jonowych.
Związki jonowe w stanie stałym tworzą kryształy jonowe, składające się z naprzemiennie ułożonych anionów i kationów. Jony ułożone są w taki sposób, aby jak największa liczba jonów jednego znaku otaczała każdy z jonów przeciwnego znaku, co jest równoznaczne z osiągnięciem najmniejszej energii. Miejsca zajmowane przez jony to węzły sieci krystalicznej. Liczbę jonów przeciwnych otaczających dany jon opisuje się za pomocą liczby koordynacyjnej, zależnej od stosunku wielkości anionu do kationu. Na przykład dla NaCl liczba koordynacyjna L.K.= 6.
Kryształy jonowe nie przewodzą prądu, natomiast ciekłe lub rozpuszczone związki jonowe tworzą elektrolity, w których prąd przenoszony jest przez przepływ kationów i anionów, podobny do ruchu elektronów w przewodnikach. Jest to możliwe dzięki temu, że substancje jonowe ulegają dysocjacji.
Związki jonowe dobrze rozpuszczają się w rozpuszczalnikach polarnych - głownie w wodzie, natomiast nie rozpuszczają się w niepolarnych rozpuszczalnikach - eterach czy benzynie.
Ze względu na małą energię wiązania, związki jonowe reagują bardzo szybko, w przeciwieństwie do związków kowalencyjnych. Mimo słabego charakteru wiązania, mają jednak wysokie temperatury wrzenia i topnienia - np. dla NaCl tt = 801°C, a tw = 1413°C.
Wiązania metaliczne powstaje w wyniku elektrostatycznego oddziaływania kationów metalu w węzłach sieci krystalicznej z gazem elektronowym elektronów walencyjnych. Substancje metaliczne są świetnymi przewodnikami elektrycznymi i termicznymi, mają również, w zależności od składu chemicznego, różne właściwości mechaniczne.

http://www.chemguide.co.uk
Wiązanie koordynacyjne (donorowo - akceptorowe) tworzy się w wyniku oddziaływania dwu atomów z parą elektronową pochodzącą od jednego z nich - donora. Wiązanie takie ma właściwości bardzo podobne jak wiązanie kowalencyjne spolaryzowane.


