Wśród wielu rodzajów roztworów rozróżniamy m.in.:
ROZTWÓR WŁAŚCIWY - roztwór, w którym składniki substancji rozpuszczonej są bardzo rozproszona (drobiny maja rozmiar około 10-7m). Roztwory takie można spotkać, we wszystkich stanach skupienia:
- Stanie stałym (np niektóre stopy metali)
- Stanie ciekłym (np woda mineralna)
- Stanie gazowym (np powietrze)
Roztwory można podzielić ze względu na stosunek stężenia roztworu do rozpuszczalności substancji rozpuszczonej.
Wyróżniamy:
- Roztwór nienasycony- jego stężenie jest mniejsze od rozpuszczalności substancji rozpuszczonej.
- Roztwór nasycony- jego stężenie jest równe rozpuszczalności substancji rozpuszczonej.
- Roztwór przesycony- jego stężenie jest wyższe od rozpuszczalności substancji rozpuszczonej
ROZPUSZCZALNOŚĆ substancji - to maksymalna ilość substancji (wyrażona w gramach), która może rozpuścić się w 100 gramach rozpuszczalnika, tworząc nasycony roztwór (jest zależna od temperatury i ciśnienia).
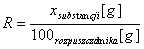
KOLOID - (inaczej nazywany układem dyspersyjnym lub układem koloidowym) - układ złożony z dwóch faz: fazy rozpraszającej (tzw. ośrodek dyspersyjny , faza ciągła) i fazy rozproszonej (tzw. faza zdyspergowana),dla której wielkość cząstek mieści się w przedziale 1 do 200 nm. Współcześnie uważa się, że aby zdefiniować koloid należy uwzględnić: rozmiar, kształt powierzchnię właściwą, gęstość oraz ładunek powierzchniowy drobin fazy rozproszonej. Powinny one być duże w stosunku do cząsteczek związków chemicznych, lecz wystarczająco małe, by siły powierzchniowe działające na granicy faz, były mocniejsze od sił ciężkości. Ta przewaga sił powierzchniowych nad bezwładnościowymi decyduje o właściwościach fizycznych koloidów. Obie fazy mogą występować w różnych stanach skupienia. Wyjątek stanowi układ gaz-gaz, tworzący zawsze mieszaninę jednorodną.
Dla koloidów charakterystyczne są:
- ruchy Browna, czyli ciągły, chaotyczny ruch drobin fazy rozproszonej
- brak możliwości przenikania przez błony półprzepuszczalne
- efekt Tyndalla- rozpraszanie światła przez cząstki fazy rozproszonej o rozmiarach mniejszych od długości fali świetlnej.
- zjawiska elektrokinetyczne (elektroforeza, elektroosmoza)
Nazwę tą stworzył Thomas Graham w roku 1861, który podzielił ciała stałe na dwa rodzaje: krystaloidy i koloidy. Według niego krystaloidy to ciała o budowie krystalicznej, tworzące po rozpuszczeniu jednorodne mieszaniny, zdolne do przechodzenia przez błony półprzepuszczalne, natomiast koloidy to ciała bezpostaciowe, które po rozpuszczeniu nie tworzą roztworów jednorodnych, a substancja rozpuszczona nie może przechodzić przez błony półprzepuszczalne.
Dziś ten podział jest nieaktualny, gdyż odkryto koloidy powstałe przez rozpuszczenie substancji krystalicznych.
Koloidy można podzielić na:
- koloidy cząsteczkowe- są fizycznie jednorodne; jednym ze składników są makrocząsteczki (duże cząsteczki np. białek), powstają przez rozpuszczanie substancji o dużych cząsteczkach.
- koloidy asocjacyjne (micelarne) - powstają przez asocjację cząsteczek
- koloidy fazowe - widoczna jest granica dwóch faz; powstają przez rozdrabnianie większych cząstek (metody dyspersyjne), prowadzące do zwiększania powierzchni właściwej lub przez wytworzenie zalążków wzrostu drobin i zahamowanie ich rozrostu, gdy osiągną rozmiary drobin charakterystyczne dla układów koloidalnych (metodami kondensacyjnymi).
Koloidy występują naturalnie (np. krew, mleko, mgła) lub są wytwarzane przez człowieka (farby, kleje, lakiery)
Koloidy, w których faza rozpraszająca jest cieczą:
- liofilowe (gdy cieczą jest woda są nazywane hydrofilowymi) - cząsteczki fazy rozproszonej wykazują duże powinowactwo do cząsteczek fazy rozpraszającej, ulęgają solwatacji (cząsteczki rozpuszczalnika oddziaływają z cząsteczkami substancji rozpuszczonej tworząc solwaty, czyli zespoły drobin obu substancji). Są termodynamicznie stabilne, do ich utworzenia nie potrzeba wykonania pracy, tworzą się samorzutnie (np. żelatyna w wodzie).
- liofobowe (gdy cieczą jest woda są nazywane hydrofobowe) - cząsteczki fazy rozproszonej wykazują małe powinowactwo do cząsteczek fazy rozpraszającej. Nie są termodynamicznie stabilne, do ich utworzenia potrzeba wykonać pracę. Układy te stabilizują się głównie dzięki jednoimiennemu ładunkowi elektrycznemu, powstającymi na powierzchni cząstek, przez co cząstki te odpychają się (np. zole metali, ich wodorotlenków i soli). Trwałość koloidów liofobowych określa się za pomocą potencjału elektrokinetycznego.
Najogólniej stabilność koloidów można wyjaśnić poprzez siły działające pomiędzy cząsteczkami: siły Van der Waalsa (o charakterze przyciągającym, dalekozasięgowe) oraz siły związane z ładunkiem elektrycznym cząstek (o charakterze odpychającym). Nakładanie się tych rodzajów sił może wyjaśnić zachowanie drobin koloidu w czasie ich wzajemnego zbliżania się. Jeśli dwie cząsteczki położone blisko siebie osiągną minimum energetyczne, to połączą się, a koloid ulegnie odwracalnej koagulacji. Jeśli natomiast taki układ pokona przewagę sił odpychających, to znajdzie się w następnym minimum energetycznym i ulegnie nieodwracalnej koagulacji.
Nazwę tą stworzył Thomas Graham w roku 1861, który podzielił ciała stałe na dwa rodzaje: krystaloidy i koloidy. Według niego krystaloidy to ciała o budowie krystalicznej, tworzące po rozpuszczeniu jednorodne mieszaniny, zdolne do przechodzenia przez błony półprzepuszczalne, natomiast koloidy to ciała bezpostaciowe, które po rozpuszczeniu nie tworzą roztworów jednorodnych, a substancja rozpuszczona nie może przechodzić przez błony półprzepuszczalne.
Dziś ten podział jest nieaktualny, gdyż odkryto koloidy powstałe przez rozpuszczenie substancji krystalicznych.
ZAWIESINA - (inaczej: suspensja, układ o rozdrobnieniu mechanicznym)- układ dyspersyjny, w którym fazą rozpraszającą jest ciecz, natomiast fazę rozproszoną stanowią rozdrobnione cząstki ciała stałego. Zawiesinę można zaliczyć do koloidów, gdy drobiny fazy rozproszonej mają rozmiary mniejsze niż 200 nm. Zawiesiny nie wykazują ruchów Browna.
Mogą istnieć także :
- zawiesiny gazowe (ośrodkiem dyspersyjnym jest gaz) - np. dym
- zawiesiny stałe (ośrodkiem dyspersyjnym jest ciało stałe)


