Promieniotwórczy izotop węgla o liczbie atomowej 14 znalazł zastosowanie w datowaniu m.in. skamieniałości organizmów roślinnych i zwierzęcych, takich wytworów działalności ludzkiej jak wyroby z drewna, skóry czy włókien roślinnych. W jaki sposób możliwe jest określenie wieku tak różnorodnych przedmiotów? Dlaczego węgiel 14C jest tak użyteczny?
Ten szczególny izotop węgla stale znajduje się w atmosferze (choć w niewielkich ilościach). Tworzy się on w wyższych warstwach atmosfery w wyniku oddziaływania neutronów z promieniowania kosmicznego na jądra atomów azotu 14N (ten izotop jest najbardziej rozpowszechnioną odmianą azotu, jest głównym składnikiem powietrza). Neutrony te dostając się do jądra atomu azotu zaburzają jego stabilność. Efektem jest wypromieniowanie protonu. W ten oto sposób jądro azotu 14N przekształca się w jądro izotopu węgla 14C. Zachodzi reakcja według równania:
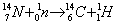
Gdy tylko powstanie nowy atom węgla promieniotwórczego niemal natychmiast zostaje utleniony do dwutlenku węgla (CO2). W atmosferze następuje równomierne wymieszanie radioaktywnego CO2 z dwutlenkiem węgla zawierającym stabilne, niepromieniotwórcze izotopy węgla ( 12C i 13C). Stąd też atmosferyczny ditlenek węgla zawiera niewielką ilość radioaktywnego ditlenku ( istotne jest że ta zawartość jest mniej więcej stała).
Rośliny asymilują dwutlenek węgla z atmosfery i na drodze fotosyntezy tworzą z niego proste substancje organiczne, które po dodatkowych modyfikacjach wbudowywane są w ich tkanki. Zwierzęta, zjadając rośliny, wykorzystują substancje w nich zgromadzone m.in. do budowy własnych tkanek. W ten sposób węgiel 14C przechodzi przez kolejne ogniwa łańcucha pokarmowego. A więc żywa materia organiczna wykazuje radioaktywność wywołaną obecnością promieniotwórczego izotopu węgla. Dopóki organizm jest żywy, wymienia z otoczeniem materię i stosunek zawartości węgla radioaktywnego do węgla o stabilnych jądrach w komórkach organizmu jest podobny jak w atmosferze. Wraz ze śmiercią, ustaje możliwość pobierania m.in. 14C z otoczenia i względna ilość tego izotopu maleje (nie ustają rozpady promieniotwórcze).
Datowanie przeprowadza się badając jak zmieniła się radioaktywność materiału. Czas połowicznego rozpadu 14C to około 5725 lat - to znaczy, że po tym czasie połowa początkowej ilości 14C rozpada się, a więc i promieniotwórczość maleje o połowę. Analizując proporcje 14C do 12C i 13C razem wziętych szacuje się wiek badanego przedmiotu (aby uzyskać dokładniejszy wynik trzeba jeszcze uwzględnić kilka poprawek). Ta metoda pozwala datować obiekty, których wiek nie przekracza 50 000 lat (wg Linus Pauling, Peter Pauling „Chemia” PWN, Warszawa 1983)


