Już od najdawniejszych czasów ludzie starali się zrozumieć i poznać jak zbudowana jest otaczająca ich materia. Jeszcze w starożytności pojawiły się różne teorie na ten temat, mówiące między innymi o tym, iż materia zbudowana jest z żywiołów. Jednak już około 420r.p.n.e. Leukippos z Miletu i Demokryt z Abdery wysnuli teorię, która głosiła, iż wszystko na świecie składa się z małych, niepodzielnych cząstek zwanych atomami. Uczeni ci twierdzili, że atomy są tworami wiecznymi i niezmiennymi, i że pozostają ciągle w ruchu. Ruch ten stanowić miał przyczynę wszelkich zmian zachodzących w przyrodzie. Przez długi czas teoria ta nie zyskiwała powszechnego uznania. Dopiero w pierwszych latach XIX wieku John Dalton po wielu latach pracy sformułował założenia nowoczesnej teorii atomistycznej, której podstawowym założeniem było przyjęcia, iż wszystkie substancje zbudowane są z niepodzielnych cząstek - atomów. Uznał on, że atomy tej samej substancji (pierwiastka) są jednakowe i mają w związku z tym identyczne masy, zaś atomy różnych pierwiastków mają masy różne. Jednak wkrótce okazało się, że hipoteza zakładająca niepodzielność atomu była fałszywa. W 1897 roku angielski fizyk, J. J. Thomson stwierdził istnienie ujemnie naładowanej cząstki, którą nazwał elektronem. Już w roku 1906 Thomson przedstawił własny model przedstawiający budowy atomu. Według niego atom był kulą, wypełnioną dodatnio naładowaną materią, a ujemnie naładowane elektrony miały być przypadkowo zanurzone w tej kuli, tak jak „rodzynki w cieście”. W roku 1911 współpracownik Thomsona, Ernest Rutherford zaprezentował wyniki swoich badać. Twierdził on, że dodatni ładunek w atomie jest skupiony w centralnie położonym, ciężkim jądrze, wokół którego krążą lekkie cząstki naładowane ujemnie (elektrony). Rutherford przyjął, że niemal cała masa atomu skupiona jest zawsze w jądrze atomowym. W roku 1913 Niels Bohr przedstawił nową teorię budowy atomu nazwaną teorią orbit stacjonarnych. Zakładał on, że wokół centralnie umieszczonego, dodatnio naładowanego jądra krążą ujemnie naładowane elektrony, poruszające się po ściśle określonych, kołowych orbitach. Model budowy atomu jest od tego czasu ciągle modyfikowany i udoskonalany przy pomocy metod mechaniki kwantowej. Jednak już w momencie ogłoszenia modelu Rutherforda uczeni zaczęli przeczuwać, iż w jądrach atomów może tkwić wielka energia. Nie zdawali sobie jednak sprawy, jak tego dokonać. Wkrótce okazało się, że również samo jądro atomowe jest strukturą złożoną i składa się z cząstek dodatnich oraz obojętnych. Cząstki dodatnie odkrył sam Rutherforda, jeszcze w roku 1919. Nazwano te cząstki protonami. W roku 1932 dokonano przełomowego odkrycia. James Chidwick wykazał, że w jądrze oprócz dodatnio naładowanych protonów występują również cząstki obojętne. Nazwane one zostały neutronami. Odkrycie to wywołało spore poruszenie w gronie fizyków atomowych. Wydawało im się, że z dużym prawdopodobieństwem wiedza ta pozwoli im wkrótce na wnikniecie w głąb jąder atomowych, a co za tym idzie wyzwolenie zmagazynowanej w nich energii.
Jak już wcześniej wspomniano, jądro atomowe jest dodatnio naładowaną częścią atomu. Skupiona jest w nim niemal cała masa atomu (dla przykładu najlżejsze jądro atomowe jest 1836 razy cięższe od elektronu), a średnica jest około sto tysięcy razy mniejsza od średnicy całego atomu. W skład jądra wchodzą dodatnio naładowane protony, oraz obojętne elektrycznie neutrony. Oba rodzaje cząstek z racji tego, iż występują w jądrach atomowych są również nazywane nukleonami. Liczba protonów w jądrze danego atomu, jest równa liczbie atomowej tego atomu (Z), a także określa ładunek jądra. Określa również położenie danego pierwiastka w układzie okresowym. Suma protonów i neutronów określa liczbę masową atomu (A). Zbiór identycznych atomów (o takich samych liczbach Z i A) nazywany jest nuklidem. Nuklidy o takich samych wartościach liczby A, lecz różnych wartościach liczby Z nazywane są izobarami. Gdy atomy mają takie same liczby Z, ale różne liczby A (czyli różnią się liczbą neutronów w jądrze atomowym) to wówczas nazywane są one izotopami. Gdy jądra danych atomów mają tę samą liczbę neutronów, ale różnią się liczbą protonów, wówczas nazywa się je izotonami.
Dokładne określenie struktury dowolnego jądra atomowego nie jest niestety możliwe przy obecnym stanie wiedzy. Naukowcy stworzyli jednak kilka modeli opisujących w przybliżeniu zachowanie się jąder atomowych. Jednym z pierwszych modeli był tzw. model kroplowy. Zakłada on, że protony i neutrony w jądrze zachowują się tak jak cząsteczki w cieczy. W związku z tym własności jądra powinny być analogiczne do własności kropli cieczy. Oddziaływania pomiędzy nukleonami są w tym modelu przedstawiane analogicznie do sił lepkości i napięcia powierzchniowego w cieczach. Model ten jest jednak bardzo przybliżony i nie pozwala na pełne wyjaśnienie własności jąder atomowych. Tzw. model powłokowy jądra atomowego zakłada, że nukleony mogą wewnątrz jądra przyjmować te stany energetyczne, które są zgodne z energiami kolejnych powłok. Model ten zakłada również, że nukleony poruszają się w jądrze prawie niezależnie od siebie. Model powłokowy pozwala na wyjaśnienie odstępstw rzeczywistej energii wiązania jąder od energii obliczonej w oparciu o model kroplowy. Pozwala on również na wyjaśnienie istnienia tzw. ”liczb magicznych”. Okazuje się bowiem, że jądra zawierające 2, 8, 20, 28, 50, 82, 126 protonów lub neutronów wykazują największe siły wiązania. Jeżeli jądro posiada jeden nukleon mniej lub więcej, to energia wiązań jest zdecydowanie mniejsza. Gdy zarówno liczba protonów jak i neutronów w jądrze danego atomu jest magiczna to nazywa się takie jądro „podwójnie magicznym”. Tzw. modele kolektywne z kolei zakładają, że nie wszystkie zjawiska jądrowe można wytłumaczyć wyłącznie przy pomocy oddziaływania nukleonów. Według tych modeli nukleony łączą się wewnątrz jądra w grupy tworząc nowe cząstki, o odmiennych właściwościach.
Enrico Fermi, prowadząc swoje badania bombardował uran powolnymi neuronami. Wyniki tych doświadczeń mogły wskazywać na powstawanie z uranu innych pierwiastków. Dopiero w roku 1939 niemieccy naukowcy stwierdzili, że jedynym z produktów powstających podczas bombardowania uranu neutronami jest bar. Okazało się więc, że można przeprowadzać udane rozszczepienia niektórych jąder atomowych i uzyskać w ten sposób duże ilości energii. Energia ta mogła zostać wytworzona albo w sposób kontrolowany, (co dziś stosuje się w reaktorach jądrowych), a także w sposób całkowicie niekontrolowany (działanie bomby atomowej).
Aby reakcja rozszczepienia mogła przebiegać w sposób łańcuchowy, tzn. by każde rozszczepienie jednego jądra inicjowało kolejne rozszczepienia, ilość rozszczepialnego pierwiastka musi być wystarczająco duża. Ta ilość nazywana jest masa krytyczną.
Jak już wcześniej wspomniano, neutrony związane są w jądrze przy pomocy wielkich sił, a ich uwalnianie powoduje wyzwolenie ogromnych ilości energii. Zgodnie z teorią Alberta Einsteina, masa i energia powiązane są ze sobą poprzez zależność:
E = m ∙ c2
Gdzie: E - energia,
m - masa,
c - prędkość światła
Ponieważ wartość czynnika c jest bardzo duża (299792458 m/s w próżni), nawet niewielki ubytek masy powoduje wydzielenie ogromnych ilości energii.
Badania nad promieniotwórczością wykazały, że atomy niektórych pierwiastków wysyłają przede wszystkim 3 rodzaje promieniowania – α, β i γ. Każde z nich ma inny zasięg, różna jest także ich przenikliwość, oraz sposób oddziaływania z polem elektrycznym. Promieniowaniem o najmniejszym zasięgu, wynoszącym jedynie kilka centymetrów w powietrzu jest promieniowanie α. Jego przenikliwość również jest niewielka. W polu elektrycznym, cząstki α odchylają się w stronę bieguna ujemnego. Promieniowanie α jest niczym innym, jak strumieniem jąder helu składających się z dwóch neutronów, oraz dwóch neutronów. Wynika więc z tego, iż masa tych cząstek jest dość wysoka. Kolejnym rodzajem promieniowania jest promieniowanie β. W polu elektrycznym promieniowanie to będące w rzeczywistości strumieniem elektronów, odchyla się w stronę bieguna dodatniego. Ma zdecydowanie większy zasięg niż promieniowanie α. Charakteryzuje się także większą przenikliwością. Niekiedy zamiast elektronu mole zostać wyemitowana cząstka o masie równej masie elektronu, ale o ładunku dodatnim. Taka cząstka nosi nazwę pozytonu, a promieniowanie określa się symbolem β+. Trzecim rodzajem promieniowania jest promieniowanie γ. W odróżnieniu od dwóch pozostałych, jest to promieniowanie elektromagnetyczne o bardzo małej długości fali, charakteryzujące się dużym zasięgiem i bardzo wysoką przenikliwością. Może zostać zatrzymane jedynie w wyniku bezpośredniego zderzenia z innym atomem.
Wydzielanie promieniowania α i β prowadzi do zmiany składu jądra atomowego. Jeżeli z jądra danego pierwiastka wyemitowana zostaje cząstka α (jądro helu), to wówczas liczba masowa atomu ulegnie zmniejszeniu o 4 jednostki, ponieważ ubywają 2 protony i 2 neutrony. Również liczba atomowa ulegnie zmniejszeniu o 2 jednostki na skutek emisji 2 protonów. Nowo powstały pierwiastek będzie się więc znajdował w układzie okresowym o dwie pozycje na lewo w stosunku do pierwiastka wyjściowego. Przemianę α można zatem zapisać schematycznie w następujący sposób.
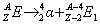
Podczas przemiany β- neutron ulega rozpadowi, w wyniku którego powstaje emitowany na zewnątrz elektron i nowy proton.
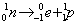
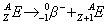
Powoduje to zwiększenie liczby atomowej nowopowstałego atomu o jeden w stosunku do atomu wyjściowego, a co za tym idzie przesunięcie w układzie okresowym o jedno miejsce w prawo.
Podczas przemiany β+ proton ulega rozpadowi, w wyniku którego powstaje emitowany na zewnątrz pozyton i nowy neutron.
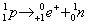
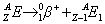
Powoduje to zmniejszenie liczby atomowej nowopowstałego atomu o jeden w stosunku do atomu wyjściowego, a co za tym idzie przesunięcie w układzie okresowym o jedno miejsce w lewo.
Opisane powyżej prawidłowości zostały odkryte niemal jednocześnie przez naukowca amerykańskiego polskiego pochodzenia – Kazimierza Fajansa oraz przez angielskiego chemika Fredericka Soddy’ego.
Reakcje jądrowe to przemiany jądrowe, które zwykle wywołane są przez cząstki padające na jądra atomowe. Cząstkami wywołującymi reakcję mogą być np. neutrony, protony, promieniowanie γ, cząstki α, a także jądra innych, lekkich pierwiastków. Wiele reakcji jądrowych przebiega w uproszczeniu w następujący sposób. W początkowym etapie reakcji cząstka padająca zostaje wychwycona przez jądro. Rezultatem tego procesu jest powstanie nowego jądra, zwanego jądrem złożonym. Takie jądro złożone zwykle jest bardzo nietrwałe i krótkim czasie ulega rozpadowi. Produktem takiego rozpadu może być jądro pierwotne, oraz identyczna cząstka, jak cząstka padająca, ale mająca mniejszą energie. W takiej sytuacji powstałe jądro będzie znajdowało się w stanie wzbudzonym. Do stanu podstawowego może następnie powrócić emitując jednocześnie kwant promieniowania γ. Tego typu reakcje nazywane są rozpraszaniem niesprężystym. Jądro złożone może również przejść do niższego stanu energetycznego nie ulegając przy tym rozpadowi a jedynie emitując kwant promieniowania γ. Może również wyemitować cząstkę inną niż cząstka padająca, a wynikiem takiej reakcji będzie jądro końcowe inne niż jądro początkowe. Mówi się wówczas o tzw. transmutacji jądra. Istnieją także reakcje tzw. rozszczepienia wymuszonego, w których jądro złożone ulega rozszczepieniu na dwa, a nawet kilka fragmentów. Bardzo istotną rolę spełniają reakcje syntezy, podczas których z dwóch jąder pierwiastków lekkich powstaje jądro pierwiastka cięższego, oraz często kwant promieniowania γ. Oczywiście reakcje jądrowe mogą wykazywać inny, mniej lub bardziej złożony przebieg i zachodzić np. z pominięciem stadium jądra złożonego (tzw. reakcje bezpośrednie).
Wszystkie reakcje jądrowe można podzielić na reakcje egzotermiczne i endotermiczne. Reakcja jest egzotermiczna wówczas, gdy całkowita energia spoczynkowa produktów końcowych przemiany jest mniejsza niż energia spoczynkowa substratów wyjściowych. Zgodnie z wyrażeniem E=m∙c2 również masa spoczynkowa produktów końcowych jest w tej sytuacji mniejsza od masy spoczynkowej substratów wyjściowych. Wynika z tego, iż podczas reakcji egzotermicznych, część energii spoczynkowej substratów ulega zmianie na energię ruchu. Typowymi przykładami tego typu procesów są między innymi rozpady promieniotwórcze, a także reakcje rozszczepienia. Reakcja jest endotermiczna, w momencie, gdy całkowita energia spoczynkowa produktów końcowych reakcji jest większa niż energia spoczynkowa substratów wyjściowych. W związku z powyższym w wyniku zajścia reakcji endotermicznej masa spoczynkowa ulega zwiększeniu.
Aby padająca cząstka mogła zapoczątkować reakcję jądrową, musi ona wniknąć do samego jądra. Problemów nie powinno być z przedostaniem się do jądra neutronów, ze względu na to, iż nie posiadają one ładunku elektrycznego. Samo jądro naładowane dodatnio działa jednak odpychająco na cząstki o ładunku dodatnim, takie jak protony, czy jądra lekkich pierwiastków. Aby mogły one pokonać te siły odpychania i wniknąć do jądra muszą posiadać bardzo dużą energię. Właśnie do przyspieszania tych cząstek służą odpowiednie urządzenia zwane akceleratorami. Najprostszym z akceleratorów jest tzw. akcelerator elektrostatyczny, składający się z długiej rury, wewnątrz której panuje próżnia. Na końcach tej rury utrzymana jest ogromna różnica potencjałów (rzędu wielu tysięcy Voltów), która powoduje przyspieszanie poruszających się wewnątrz cząstek naładowanych.
Reakcje łańcuchowe z rozszczepieniami jądrowymi, zachodzące w sposób całkowicie kontrolowany znalazły szerokie zastosowanie jako źródło energii o ogromnej wydajności. Wykorzystuje się je między innymi w elektrowniach jądrowych. Urządzenia, w których przeprowadza się kontrolowane reakcje łańcuchowe, nazywane są reaktorami jądrowymi. Jako materiał rozszczepialny stosuje się między innymi uran, ale w normalnych warunkach może nie zostać zainicjowana reakcja łańcuchowa. Korzysta się wówczas z tzw. moderatora, który jest substancja zawierającą atomy lekkich pierwiastków. Moderator jest wprowadzany do reaktora w odpowiednich ilościach właśnie w celu zapoczątkowania reakcji łańcuchowej. Ważnymi i niezbędnymi elementami każdego reaktora jądrowego są urządzenia, które zabezpieczają przed zbyt intensywnym wzrostem szybkości reakcji łańcuchowej. Najczęściej wykorzystywane są w tym celu pręty kadmowe, ponieważ jądra kadmu mają szczególną zdolność toteż wychwytywania neutronów, spowalniając tym samym reakcje poprzez uniemożliwianie dalszych rozszczepień. W reaktorze wydzielana jest energia cieplna, która następnie jest przejmowana przez czynnik chłodzący (zwykle gaz lub ciecz przepływającą przez reaktor) i odprowadzana na zewnątrz. W różnych typach używanych reaktorów stosowane są różne paliwa jądrowe, a także różne rodzaje moderatorów i różne czynniki chłodzące, w zależności od zastosowanych rozwiązań konstrukcyjnych. Reaktory można podzielić na trzy podstawowe grupy w zależności od ich przeznaczenia. Powszechnie w wielu krajach są stosowane reaktory służące jako źródła energii. Inne reaktory mogą być przeznaczone do badań naukowych z dziedziny fizyki i chemii. Trzecią grupę stanowią reaktory mogące służyć do sztucznych izotopów promieniotwórczych, a w szczególności nowych substancji mogących ulegać rozszczepianiu. Przykładem może być produkcja plutonu z naturalnego uranu.
Izotopy promieniotwórcze, zarówno te występujące w naturze, jak i te otrzymywane sztucznie, mają bardzo szerokie zastosowanie w różnych dziedzinach życia. Jak już wcześniej wspomniano, promieniotwórczość jest zjawiskiem samoistnej przemiany jąder atomowych w inne jądra, a głównymi procesami zachodzącymi podczas przemiany promieniotwórczej są opisane powyżej rozpad beta, rozpad alfa, a także wychwyt elektronu oraz spontaniczne rozszczepienie. Intensywność procesu promieniotwórczego opisywana jest przy pomocy tzw. aktywności promieniotwórczej danej substancji. Najważniejszą wielkością charakteryzującą dany izotop promieniotwórczy jest tzw. czas połowicznego zaniku (okres połowicznego rozpadu, okres półtrwania). Jest to czas, po jakim połowa początkowej ilości danego izotopu promieniotwórczego ulegnie rozpadowi. Ogólnie przyjmuje się, że całkowity rozpad danego radioizotopu zachodzi po upływie czasu równego pięciu okresom półtrwania. Czas połowicznego rozpadu jest dla danego izotopu wielkością niezależną od czynników zewnętrznych, takich jak temperatura, ciśnienie itp. Oznacza się go zwykle symbolem T1/2. Inną wielkością charakteryzująca rozpad promieniotwórczy danego izotopu jest tzw. stała rozpadu oznaczana literą λ. Określa ona prawdopodobieństwo zajścia rozpadu promieniotwórczego jednego jądra w jednostce czasu. Obie te wielkości powiązane są ze sobą następującą zależnością:
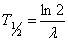
Czasami wprowadza się jeszcze pojecie biologicznego czasu połowicznego zaniku. Odpowiada on czasowi, po jakim następuje zmniejszenie aktywności danego radioizotopu wchłoniętego do organizmu do połowy jego wartości początkowej. Dla różnych pierwiastków promieniotwórczych okresy połowicznego rozpadu wahają się od ułamków sekund do nawet miliardów lat. Pod względem możliwości praktycznego zastosowania, największe znaczenie mają rozszczepienia jąder uranu i plutonu, ponieważ izotopy 235U, 233U a także 239Pu mogą ulegać rozszczepieniu już podczas bombardowania neutronami o bardzo niskiej energii. Pojedyncze rozszczepienie jądra atomowego może w pewnych warunkach powodować dalsze rozszczepienia, co prowadzić może do zainicjowania reakcji łańcuchowej, o której już była mowa.
Ważnym pojęciem z zakresu promieniotwórczości jest tzw. „szereg promieniotwórczy”. Jest to zespół pierwiastków promieniotwórczych, które powstają w wyniku następujących jeden po drugim rozpadów promieniotwórczych. Produkty kolejnych rozpadów tworzą szereg. Na początku tego szeregu znajduje się izotop promieniotwórczy o dość długim okresie półtrwania, a na końcu izotop trwały, nieulegający rozpadowi. Tradycyjnie rozróżnia się cztery szeregi promieniotwórcze.
- Szereg uranowo radowy - rozpoczyna się rozpadem alfa izotopu 238U, a kończy trwałym izotopem ołowiu 206Pb.
- Szereg uranowo aktynowy – rozpoczyna się rozpadem izotopu 235U, a kończy trwałym izotopem ołowiu 207Pb
- Szereg torowy – rozpoczyna się rozpadem izotopu toru 232Th, a kończy stabilnym izotopem 208Pb
- Szereg neptunowy – rozpoczyna się rozpadem izotopu neptunu 237Np, a kończy stabilnym bizmutem 209Bi
Trzy pierwsze występują w środowisku naturalnym. Szereg neptunowy, występował we wczesnym okresie istnienia Ziemi. Ostatnio pojawił się jednak ponownie ze względu na obecność zanieczyszczeń promieniotwórczych, przede wszystkim izotopem 241Pu, który rozpada się na 241Am, a następnie tworząc 237Np.
Naturalne izotopy promieniotwórcze wykorzystywane są między innymi w geologii między innymi do określania przybliżonego wieku skał. Bardzo popularną metodą określania wieku szczątków materii organicznej jest metoda radiowęglowa, wykorzystująca właściwości izotopu 14C. Dokonując pomiaru zawartości tego izotopu w próbce materii organicznej, można przybliżoną datę „śmierci” badanego organizmu.
Zastosowanie sztucznych izotopów promieniotwórczych, otrzymywanych w specjalnie do tego celu przeznaczonych reaktorach jądrowych, jest również bardzo szerokie. Izotopy te przede wszystkim są cennym źródłem promieniowania. Ze względu na silne właściwości bakteriobójcze, promieniowanie γ stosuje się często do sterylizacji, przede wszystkim produktów spożywczych. Również w medycynie wykorzystuje się fakt, że komórki nowotworowe pod wpływem promieniowania γ ulegają zniszczeniu dużo szybciej, niż otaczające je komórki zdrowe. Radioizotopy nie tylko wykorzystuje się w medycynie do leczenia nowotworów. Również wiele badań diagnostycznych korzysta z promieniowania emitowanego przez podane do organizmu chorego substancje promieniotwórcze. Kwanty promieniowania γ charakteryzują się wystarczająco dużą przenikliwością i dostatecznie dużą energią, aby przeniknąć nawet przez dość grube warstwy metalu. Wykorzystuje się to do wykrywania wad różnych materiałów, stosowanych następnie do różnych celów.
Bardzo istotne znaczenie w wielu badaniach naukowych zyskała tzw. metoda atomów znaczonych. Wykorzystuje ona fakt, iż wszystkie izotopy danego pierwiastka charakteryzują się jednakowymi właściwościami chemicznymi. Zamieniając poszczególne atomy danego pierwiastka izotopami promieniotwórczymi, można śledzić przemieszczanie się tych atomów podczas zachodzących procesów. Pozycje atomów promieniotwórczych określa się oczywiście przy pomocy pomiaru natężenia emitowanego przez nie promieniowania. W ten sposób bada się mechanizmy wielu reakcji chemicznych, a także procesów biochemicznych, zachodzących w organizmach żywych.
Jak już wcześniej wspomniano największe zastosowanie izotopów promieniotwórczych wiąże się z uzyskiwaniem wielkich ilości energii z reakcji rozszczepienia bardzo ciężkich jąder atomowych (np. uranu, plutonu, toru) lub z syntezy lekkich pierwiastków (jak hel, lit). Pierwsze elektrownie jądrowe pojawiły się już w latach pięćdziesiątych ubiegłego stulecia. Stopniowy wzrost znaczenia energetyki atomowej wiąże się oczywiście z faktem, iż wykorzystywane w celach energetycznych surowce, jak węgle kopalne, ropa naftowa, czy gaz ziemny, mogą za jakiś czas ulec wyczerpaniu. Również produkcja energii przy pomocy reaktorów jądrowych nie powoduje emisji szkodliwych substancji do atmosfery. Wydajność elektrowni jądrowych jest poza tym nieporównywalnie większa, niż klasycznych i pozwala na uzyskanie dużych ilości energii znacznie mniejszym kosztem. Elektrownia jądrowa jest zazwyczaj połączeniem reaktora jądrowego z elektrownią cieplną. Uzyskiwana moc zależy przede wszystkim od rodzaju reaktora, ale również od wykorzystywanej metody chłodzenia. Uzyskiwane ciepło jest następnie zamieniane na energię elektryczną.
Największe niebezpieczeństwo wiąże się z wykorzystaniem reakcji jądrowych do produkcji broni masowego rażenia. W reaktorach stosowanych w elektrowniach jądrowych, reakcje przebiegają w sposób kontrolowany, a wielka ilość zabezpieczeń nie dopuszcza do zainicjowania lawinowej reakcji łańcuchowej. W przypadku broni jądrowej zachodzące procesy rozpadu promieniotwórczego nie są w żadnym stopniu kontrolowane. Reakcja łańcuchowa powoduje wydzielenie ogromnych ilość energii. Wysoka temperatura oraz energia produktów rozpadu powodują rozproszenie materiału, a następnie przerwanie reakcji łańcuchowej. W wyniku wybuchu jądrowego powstaje ogromna fala uderzeniowa, niszcząca niemal wszystko, co napotka na swej drodze. Emitowane jest również promieniowanie, powodujące skażenie objętego wybuchem rejonu. W produkcji broni masowego rażenia wykorzystuje się również reakcje syntezy jądrowej, polegające na łączeniu się lekkich jąder atomowych w jądra cięższe. Głownie wykorzystuje się w tym celu jądra wodoru, stąd nazwa tego rodzaju broni – „bomby wodorowe”. Stosowane są także tzw. „brudne bomby”. Jest rodzaj broni radiologicznej, której działanie polega na rozrzuceniu w wyniku konwencjonalnej eksplozji na konkretnym terenie materiału radioaktywnego, który następnie powoduje skażenie promieniotwórcze terenu.
Skażenie promieniotwórcze może pojawić się również w wyniku nieodpowiedniego składowania odpadów z elektrowni jądrowych, a także w wyniku awarii reaktora. Najsłynniejsza i najniebezpieczniejsza awaria tego typu miała miejsce w Czarnobylu na Ukrainie w roku 1986. Jej skutki są widoczne do dnia dzisiejszego.
Wpływ promieniowania jonizującego na organizmy żywe zależy od pochłoniętej dawki promieniowania. Jednorazowo pochłonięta dawka około 100 siwertów, powoduje natychmiastowy zgon. Dawki rzędu kilku siwertów mogą spowodować śmierć w przeciągu kilku tygodni. Po krótkim czasie pojawiają się objawy charakterystyczne dla tzw. choroby popromiennej, tj. odwodnienie, biegunka, nudności, porażenie układu nerwowego, a następnie śmierć. Mniejsze dawki powoduję różnego rodzaju mutacje i nowotwory (między innymi białaczkę). Dzieci rodzące się na terenach skażonych często posiadają różnego rodzaju skomplikowane wady wrodzone. Przykłada się w związku z tym coraz większą wagę do systemów bezpieczeństwa stosowanych w reaktorach jądrowych. Duży nacisk kładzie się również na rozsądne gospodarowanie odpadami promieniotwórczymi, by zapobiec niekontrolowanemu skażeniu środowiska. Rządy większości krajów Świata wycofują lub ograniczają ilość posiadanej broni nuklearnej.
Obecnie obserwuje się dalszy wzrost intensywności badań nad promieniotwórczością, a szczególnie nad jej wykorzystaniem w różnych dziedzinach życia.


